V najnovejši izdaji spletne serije seminarjev CTGCT Science Talks smo gostili dr. Thomasa Foxa, zdravnika-raziskovalca, katerega delo povezuje klinično in laboratorijsko okolje med institucijama Harvard Medical School in University College London. Njegove raziskave so osredotočene na »programabilne« terapije T-celic, področje medicine, kjer se pri zdravljenju bolezni ne zanašamo več zgolj na zunanje kemikalije ali zdravila. Namesto tega se znanstveniki učijo, kako prepisati gensko kodo lastnih imunskih celic in jih spremeniti v »živa zdravila«, sposobna prepoznati in uničiti raka ali popraviti redke genetske motnje.
Človeški imunski sistem je izjemno kompleksen, vendar ni popoln. Včasih nima ustreznih mehanizmov za prepoznavanje tumorjev, drugič pa pomotoma napade lastno telo, ki bi ga moral ščititi. Delo dr. Foxa skuša te težave rešiti z uporabo tehnik genskega urejanja za spreminjanje T-celic, pomembnega dela imunskega sistema, ki ima ključno vlogo pri uravnavanju imunskih odzivov. Z združevanjem natančnosti tehnologije CRISPR za gensko urejanje ter inovativnih dostavnih sistemov, kot so lipidni nanodelci, njegova skupina razvija načine za inženiring teh celic tako znotraj telesa (in vivo) kot zunaj njega.

Popravljanje »zavor« imunskega sistema
Eden izmed osrednjih raziskovalnih fokusov dr. Foxa je redka in življenjsko nevarna genetska bolezen, znana kot pomanjkanje CTLA4 (CTLA4 insufficiency). Pri zdravem posamezniku protein CTLA4 deluje kot ključna regulatorna »zavora« imunskega sistema in skrbi, da T-celice ne postanejo prekomerno aktivne ter ne napadejo zdravih telesnih tkiv. Kadar bolniku primanjkuje proteina CTLA4, njegov imunski sistem ostane v stalnem stanju visoke pripravljenosti, kar vodi v huda vnetja, poškodbe organov in bistveno večje tveganje za razvoj raka. Dolga leta je bila edina potencialna možnost zdravljenja za te bolnike popolna presaditev kostnega mozga – visoko tvegan postopek, pri katerem se celoten imunski sistem bolnika nadomesti z donorskimi celicami.
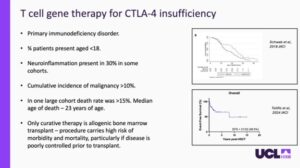
Da bi ponudili varnejšo in natančnejšo alternativo, dr. Fox in njegova skupina uporabljajo tehnologijo CRISPR-Cas9 za popravljanje bolnikovih lastnih T-celic. Najprej iz krvi bolnika izolirajo in gensko spremenijo specifično vrsto T-celic (CD3+ T-celice). Namesto da bi nov gen naključno vstavili v genom, uporabljajo tehnologijo CRISPR (»molekularne škarje«) za ciljanje specifičnega nekodirajočega dela DNK, imenovanega intron (natančneje intron 1). Običajno se ta regija med pretvorbo DNK v proteine prezre, vendar lahko z vstavitvijo zdrave kopije gena CTLA4 neposredno v to naravno regulatorno mesto celica uporabi lastne nadzorne mehanizme za uravnavanje proizvodnje proteina CTLA4 in se tako izogne tveganjem prekomerne produkcije. To je pogosta težava starejših metod genske terapije.
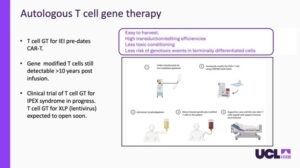
Rezultati tega pristopa so bili v predkliničnih raziskavah zelo obetavni. Ko so te spremenjene T-celice vnesli v testne modele, so potovale po telesu do prizadetih organov ter uspešno umirile prekomerno aktiven imunski sistem, kar je omogočilo celjenje otečenih in poškodovanih tkiv ter njihovo vrnitev na normalno velikost (Povezava do članka). Ta preboj je odprl pot klinični translaciji, saj je začetek kliničnega preskušanja načrtovan za maj 2028, kar bolnikom ponuja upanje za »živo zdravilo«, ki bi lahko ponovno vzpostavilo ravnovesje imunskega sistema brez potrebe po donorski presaditvi.
»Nevidne« T-celice: urejanje epitopov
Poleg popravljanja genetskih napak je dr. Fox predstavil tudi, kako narediti inženirske T-celice »nevidne«, da lahko preživijo zahtevno okolje bolnikovega telesa med zdravljenjem. Pogosto zdravniki pred vnosom novih T-celic uporabijo močna zdravila, imenovana monoklonska protitelesa, za odstranitev obstoječih okvarjenih imunskih celic in s tem ustvarijo »prostor« za nove. Težava pa je, da so ta zdravila pogosto preveč učinkovita – ne razlikujejo med »slabimi« starimi celicami in »dobrimi« gensko spremenjenimi celicami, zato lahko draga nova terapija propade takoj po aplikaciji.
Za rešitev tega problema je skupina dr. Foxa uporabila tehniko, imenovano urejanje epitopov (epitope editing). »Epitop« je v osnovi specifično mesto oziroma vezavno mesto na proteinu, na katerega se protitelo pritrdi za prepoznavo celice. Z uporabo tehnologije CRISPR za spremembo le ene ali dveh aminokislin v površinskem proteinu T-celic, imenovanem CD52, je skupina ustvarila različico proteina, ki je monoklonskim protitelesom nevidna. Medtem ko so drugi raziskovalci poskušali protein CD52 preprosto popolnoma odstraniti, je dr. Fox ugotovil, da takšen pristop »knock-out« celice dejansko naredi veliko bolj ranljive.

Razlog za to se skriva v skriti funkciji proteina CD52. Ta protein ne deluje zgolj kot tarča, temveč drugim imunskim celicam, imenovanim makrofagi, pošilja pomemben signal »ne pojej me«. Kadar je protein popolnoma odstranjen, makrofagi T-celice ne prepoznajo več kot »prijazne« in jo uničijo. S preciznim urejanjem epitopa namesto odstranitve celotnega proteina je skupina ustvarila »nevidne« T-celice, ki so bistveno bolj odporne. Te celice se lahko skrijejo pred zdravilom, hkrati pa ohranijo zaščitne signale, zaradi česar so dolgoročno veliko bolj funkcionalne in učinkovite v boju proti bolezni.
»Tovarna na mestu samem«: programiranje in vivo
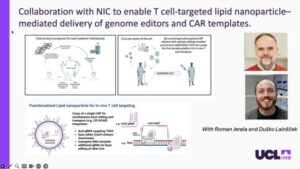
Namesto večtedenskega postopka odstranjevanja in spreminjanja T-celic v laboratoriju dr. Fox razvija »in vivo« programiranje, pri katerem T-celice gensko spreminjajo neposredno v bolnikovem telesu. V sodelovanju s prof. Romanom Jeralo, dr. Duškom Lainščkom z ter člani ekipe CTGCT uporabljajo lipidne nanodelce (mikroskopske »maščobne mehurčke«) za dostavo genskih navodil T-celicam, medtem ko so še vedno v krvnem obtoku.
Ta pristop je pokazal izjemen potencial pri rakih kostnega mozga, kot je levkemija. Ker se T-celice programirajo neposredno tam, kjer se nahaja rak, jim ni treba premagovati zahtevne poti iz krvi v globoka kostna tkiva. Dr. Fox je ugotovil, da so te »na mestu programirane« celice naravno bolj vzdržljive in učinkovite kot laboratorijsko vzgojene celice, kar bi lahko kompleksno laboratorijsko proizvodnjo spremenilo v preprosto življenjsko pomembno injekcijo.
Proti novi dobi živih zdravil
Dr. Fox je v spletnem seminarju pokazal, da je cilj njegovih raziskav preseči omejitve tradicionalne medicine z ustvarjanjem nove generacije »programabilnih« terapij. Z uporabo natančnosti sistema CRISPR-Cas9 in učinkovitosti dostave z nanodelci njegovo delo stremi k varnejšim in učinkovitejšim zdravljenjem bolnikov z agresivnimi oblikami raka ter kompleksnimi imunskimi motnjami. Ne glede na to, ali gre za popravljanje genetske »zavore«, ki prepreči, da bi telo napadalo samo sebe, ali za razvoj »nevidnih« celic, ki lahko preživijo ob uporabi močnih zdravil, ostaja cilj enak: spremeniti imunski sistem v natančno nadzorovano in usmerjeno orodje za zdravljenje.
Dr. Foxu se iskreno zahvaljujemo za delitev teh izjemnih vpogledov in za njegovo predanost premikanju meja mogočega v sodobni medicini skupaj s skupnostjo CTGCT. O nadaljnjem razvoju našega skupnega sodelovanja vas bomo še obveščali.
