Predstavljajte si, da bi se lahko s svojimi celicami pogovarjali enako kot s pametno napravo v domu. Celici bi lahko naročili, naj začne proizvajati določeno zdravilo samo takrat, ko je to potrebno, ali pa skupini celic ukazali, naj spremenijo svoje vedenje, ko zaznajo določen signal v telesu. Sintezni biologi že leta poskušajo ustvariti takšne »daljinske upravljalnike« za življenje, vendar raziskava, predstavljena v tem članku raziskovalcev iz Odseka za sintezno biologijo in imunologijo ter centra CTGCT na Kemijskem inštitutu, ta pristop dviguje na povsem novo raven. Z uporabo komponent, ki jih že najdemo v našem telesu, in fizikalnega principa, podobnega tistemu, zaradi katerega deluje lava svetilka, so raziskovalci razvili način za izjemno močno in natančno vklapljanje ter izklapljanje genov.
Ključni pojmi za razumevanje
- Kemično inducirana dimerizacija (CID): To je biološki mehanizem, pri katerem se dva proteina povežeta le v prisotnosti določene majhne molekule, encima ali drugega dimerizacijskega dejavnika. Predstavljajte si to kot molekularni sistem »ježka«, kjer dva proteinska dela ostaneta ločena, dokler ju specifična molekula – kot nekakšno lepilo – ne poveže skupaj.
- Tekoče-tekoča fazna separacija (LLPS): Gre za proces, podoben obarjanju v raztopini, vendar namesto trdne snovi podobne molekule tvorijo kapljice, ki plavajo v raztopini. Podobno kot »mehurčki« v lava svetilki.
- Biomolekularni kondenzati: To so majhni tekoči »mehurčki«, ki nastanejo zaradi LLPS znotraj celice in omogočajo, da kemične reakcije potekajo veliko hitreje, saj na majhnem prostoru združijo potrebne komponente.
- Jedrni receptorji: To so naravni človeški proteini, ki delujejo kot antene ali senzorji za prepoznavanje specifičnih hormonov in sprožijo odziv v celici.
- Transkripcija: Biološki proces »branja« genetskih navodil iz DNK, pri katerem nastane kopija v obliki RNK, ki se kasneje uporabi za tvorbo proteina. Predstavljajte si to kot digitalno fotografijo redke knjige v knjižnici: dobite informacije v uporabni obliki, ne da bi ogrozili izvirnik.
Od preprostih stikal do tekočih molekularnih elektrarn
Kar naredi to raziskavo tako inovativno, je prehod od »digitalnih« stikal k »ojačanim« sistemom. V preteklosti so znanstveniki pogosto uporabljali jedrne receptorje iz bakterij ali rastlin za gradnjo takšnih celičnih kontrolnih sistemov. Čeprav so delovali, jih je naš imunski sistem včasih prepoznal kot »tujke«, odziv, ki so ga sprožili, pa je bil pogosto šibek – kot medlo utripanje žarnice. Raziskovalna skupina na Kemijskem inštitutu se je zato odločila »preoblikovati« človeške receptorje. Vzeli so zaznavni del človeških hormonskih receptorjev (na primer za vitamin D ali estrogen) in ga spremenili v visokotehnološki sistem kemično inducirane dimerizacije (CID). Ker ti deli izvirajo iz človeka, je veliko verjetneje, da bodo varni za uporabo v medicini brez sprožitve imunskega odziva.
Prava »čarovnija« pa se je zgodila, ko so te človeške receptorje združili s konceptom tekočih kapljic. Z načrtovanjem jedrnih receptorjev z več »lepljivimi« konci (t. i. domenami za vezavo liganda) so raziskovalci ugotovili, da po dodatku hormona proteini ne tvorijo le parov, temveč preidejo v proces fazne separacije.
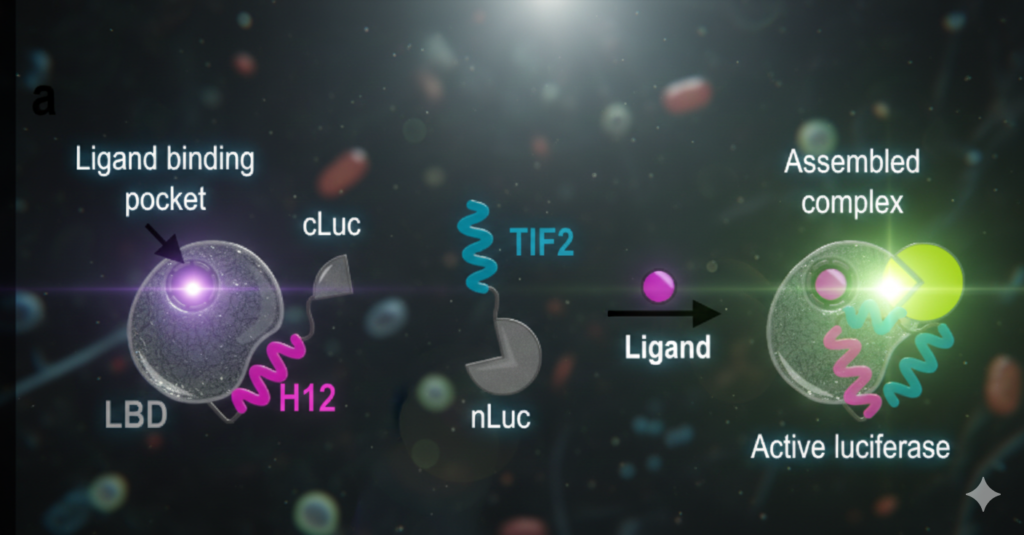
Na primer: ko se v sistem vnese hormon, kot sta kortizol ali estrogen (ligand), se ta veže na domeno za vezavo liganda na jedrnem receptorju. To povzroči strukturno spremembo v receptorju, natančneje premik dela, imenovanega Helix 12, kar razkrije »hidrofobni žleb« na površini receptorja. Ta žleb ustvari idealno okolje, da se drugi peptid v tem dimeru, imenovan TIF2, »prilepi« na jedrni receptor.
Inovacija je v tem, da so znanstveniki uporabili več ponovitev teh TIF2 peptidov (do šest zapored) in združili več domen za vezavo liganda. Ker je hkrati na voljo veliko »lepljivih« mest, proteini ne najdejo le enega partnerja in se ustavijo. Namesto tega se hitro povezujejo med seboj, izstopijo iz okoliške celične tekočine in se združijo v goste tekoče kapljice – biomolekularne kondenzate. To je proces tekoče-tekoče fazne separacije, ki učinkovito ustvari koncentrirano »reakcijsko vozlišče«, kjer se signal za aktivacijo gena ojača tudi za več sto krat.
Posledica je, da na tisoče molekul, ki aktivirajo gene, nenadoma vstopi v eno samo gosto tekočo kapljico neposredno na DNK. Tako nastane t. i. »učinek praga«. Namesto počasnega in postopnega povečevanja aktivnosti ostane izražanje gena nizko, dokler ni prisotna zadostna količina hormona za nastanek kapljice – nato pa aktivnost »eksplodira« na več sto kratnik prvotne ravni. Takšna stopnja moči in ojačanja je bila v sintezni biologiji doslej zelo težko dosegljiva.
Zakaj je ta raziskava pomembna za prihodnost
Posledice tega dela za medicino in biotehnologijo bi lahko bile izjemne. Ker so raziskovalci uporabili receptorje, ki se odzivajo na pogosta, klinično odobrena zdravila in naravne hormone, kot sta kortizol ali estrogen, imamo »daljinske upravljalnike« v bistvu že doma – v svojih omaricah z zdravili. To bi lahko vodilo do nove generacije »pametnih« celičnih terapij. Na primer: pacient bi lahko imel v telesu inženirsko spremenjene celice, ki ostanejo neaktivne, dokler ne vzame določene varne tablete, ki sproži nastanek teh tekočih kapljic in aktivira močan terapevtski odziv – samo takrat in tam, kjer je potreben.
Poleg tega je sistem popolnoma reverzibilen. Z dodatkom druge molekule, t. i. antagonista, ki blokira jedrni receptor, so raziskovalci pokazali, da lahko tekoče kapljice raztopijo in skoraj takoj izklopijo gen. Takšno »varnostno stikalo« je za medicino ključnega pomena. Z združevanjem sintezne biologije z naravnimi signalnimi sistemi telesa bi lahko ta pristop postal ključen pri oblikovanju prihodnjih terapij, ki ne bodo le močnejše, temveč tudi veliko bolj usklajene z našim imunskim sistemom – kar je osrednji cilj sodobne precizne medicine.